“減肥神藥”賣爆,全球缺貨!跨國藥企去年吸金超百億美元,中國專利存爭議
作者|杜蘇敏、鄧宇晨 來源|時代周報(ID:timeweekly)
6月3日,國家藥監局藥審中心(CDE)官網顯示,全球胰島素巨頭諾和諾德(NVO.NYSE)的司美格魯肽注射液(Ozempic,中文商品名為諾和泰)的新適應證上市申請已獲得受理。
外界普遍推測此次申報的是“減肥適應癥”,即作為低卡路里飲食和增加體力活動的輔助治療用于初始體重指數BMI≥30kg/㎡(肥胖),或27kg/㎡≤BMI<30kg/㎡(超重)并且伴有至少一種與超重相關合并癥的成人患者。
 △ 圖片來源:諾和諾德
△ 圖片來源:諾和諾德
時代周報記者從業內人士處了解到,一款新藥的上市申請從獲受理到正式獲批要近2年的時間,而對于新增適應癥的產品,審批時間有望縮短一半。也就是說,如果一切順利的話,可用來減重的司美格魯肽注射液最快一年內就能在國內獲批上市。
不過,該適應癥對適用人群仍然有著嚴格的要求,首先為成人患者,且患者的初始體重指數要≥27kg/㎡。這意味著,健康人士單純出于減肥目的使用司美格魯肽注射液,仍屬于超適應癥范疇。
然而,因減肥效果更好、副作用更小,近年來,司美格魯肽已風靡富豪圈和明星圈,特斯拉創始人埃隆·馬斯克曾自爆使用司美格魯肽一月瘦了18斤。由此,司美格魯肽已被冠上“減肥神藥”的稱號。超高的熱度和廣闊的市場前景也助長了國內外藥企的熱情,GLP-1靶點藥物成為近年糖尿病和醫美賽道的研發熱點。
“這個靶點實在太火,也有很硬的邏輯存在,會成為爆款。”6月5日,在上市藥企從事GLP-1藥物研發的李鳴(化名)告訴時代周報。
目前,諾和諾德原研的初代產品利拉魯肽已過專利保護期,多家國內藥企已入局研發。由華東醫藥(000963.SZ)生產的首款國產利拉魯肽注射液已于2023年上市。此外,司美格魯肽化合物的中國專利期限也將于2026年到期(2022年其中國專利被判無效),這無疑刺激了更多企業入局。
據時代周報不完全統計,除了華東醫藥外,包括信達生物(01801.HK)、恒瑞醫藥(600276.SH)、通化東寶(600867.SH)翰宇藥業(300199.SZ)、眾生藥業(002317.SZ)、麗珠集團(000513.SZ)、聯邦制藥(3933.HK)等多家企業紛紛展開了以GLP-1為靶點的仿制藥或創新藥研發。
一
司美格魯肽陷產能困境
目前,諾和諾德旗下共有3款司美格魯肽藥物獲得FDA批準,分別是降糖藥司美格魯肽注射液Ozempic、口服降糖藥司美格魯肽片Rybelsus、減肥藥司美格魯肽注射液Wegovy。
2021年4月,司美格魯肽注射液Ozempic首次在中國獲批上市,對應適應癥為用于改善2型糖尿病患者的血糖控制,劑型分別為1.5ml和3ml,兩款規格均為1.34mg/ml。同年6月,規格為2.4mg/0.75ml的司美格魯肽注射液Wegovy在美國獲批用于成人肥胖癥,成為全球首個用于體重管理的GLP-1受體激動劑。
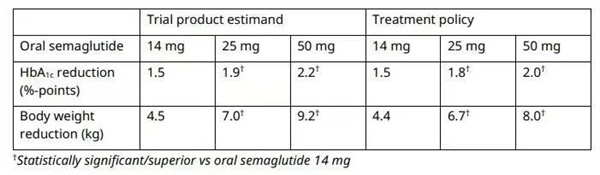 △ Rybelsus的IIIb期研究結果,圖片來源:諾和諾德官網
△ Rybelsus的IIIb期研究結果,圖片來源:諾和諾德官網
相較于初代產品利拉魯肽需要每天注射,司美格魯肽一周注射一次且效果更好,因而讓GLP-1受體激動劑實現了真正的市場爆發。
2022年8月,有消息稱司美格魯肽注射液在中國減肥適應癥的III期臨床已完成。公開報道顯示,該試驗(CTR20202040)是一項隨機、雙盲、國際多中心的III期臨床,旨在評估與安慰劑組相比,每周1次皮下注射的司美格魯肽(24mg)在超重/肥胖同時患有或未患有2型糖尿病患者中的有效性和安全性。國內共入組300例患者,國際為375例。試驗的主要終點為第44周時體重較基線的變化(%)和44周后達到體重減輕≥5%的患者比例。次要終點包括44周后達到體重減輕>10%,體重減輕≥15%,以及第44周時腰圍、收縮壓、身體功能評分與身體功能領域評分的變化等。
關于司美格魯肽減肥適應癥何時能獲批的問題一直備受業內關注。國家藥監局藥品審評中心高級審評員張杰在首屆中國糖尿病和代謝性疾病藥物器械研發創新大會上被問及相關問題時曾表示:“我們會按照正常的審評程序審批,具體的獲批速度不是我們能決定的,因為企業還沒有正式申報。”
李鳴告訴時代周報記者,諾和諾德之前的國際多中心臨床已經納入了中國受試者,目前數據完善就可以申報了。“這個申報感覺只是走個流程,沒有按照很趕的節奏去做。可能他們一方面還在缺貨,另一方面是大量的超適應癥使用,不愁賣。”
李鳴也認為,司美格魯肽注射液新增適應癥的審批預計一年內可以完成。“司美格魯肽注射液前面做過審評,很多數據和糖尿病適應癥是一樣的,無需再復核,主要是臨床數據的審核。另外,如果換了包材,可能會增加一點審核時間。”他進一步解釋道。
盡管減肥適應癥在多國未獲批,但在“減肥”效果的加持下,司美格魯肽系列產品銷售火爆,徹底點燃了減肥藥的市場需求,甚至出現了全球性的供應短缺。據報道,中國、美國、澳大利亞、歐洲等國家和地區均出現了缺貨、斷貨的現象。
2022年4月,澳大利亞藥物管理局開始不斷收到來自患者及醫生群體反饋的司美格魯肽注射液短缺信息。2023年3月,歐洲藥品管理局發布的官方聲明也指出,諾和諾德的司美格魯肽注射液將面臨較長時間的供應短缺,并且預計這種短缺將持續一整年。歐洲藥品管理局補充稱,雖然對司美格魯肽的供應將繼續增加,但不確定何時才能滿足市場需求。
司美格魯肽產能問題一直困擾著諾和諾德。今年5月,諾和諾德宣布將Wegovy在美國針對新患者的起始劑量供應量減半,以應對市場供不應求的壓力。
諾和諾德旗下司美格魯肽產品的第一家合同制造商為全球CDMO龍頭Catalent。但2021年10月,Catalent位于比利時布魯塞爾的工廠因灌裝線上的污染管控不當遭到FDA指控,這或許加劇了Wegovy的供應困境。同年12月諾和諾德透露,一家為GLP-1藥物進行注射器灌裝的合同制造商停止了交付。
隨后,諾和諾德多次宣布增加投資擴建或新建其在丹麥卡倫堡、Bagsvaerd和美國克萊頓的工廠,以提升原料藥的產能以及組裝和包裝的能力。不過,由于GLP-1受體激動劑屬于多肽類型,工藝要求較高,因此司美格魯肽全球供應緊張的問題并未解決。
今年4月,諾和諾德與第二家合同制造商簽約,承諾增加Wegovy的供應,而第三家合同制造商也將在今年晚些時候開始生產司美格魯肽產品,供應問題或將得到緩解。
二
國內上百藥企圍攻GLP-1賽道
“司美格魯肽的藥理機制為通過刺激腸促胰素,即GLP-1受體,進而增加胰島素的分泌,以及抑制胰高血糖素的分泌,從而達到降糖的目的。另外,司美格魯肽還可以作用于人體下丘腦的進食中樞,抑制食欲,減緩胃的排空,達到降低體重的作用。”廣州中醫藥大學第一附屬醫院白云醫院重癥醫學科負責人彭曉紅告訴時代周報記者。
司美格魯肽作為“減肥神藥”的出圈,加之專利期限將至,直接帶火了國內GLP-1藥物開發賽道。在海外藥企巨頭加緊完善其產品體系及新適應癥申報的同時,國內的大型藥企乃至初創藥企也都在“摩拳擦掌”。
Insight數據庫顯示,目前全球共有289個GLP-1受體激動劑處于臨床前至批準上市階段,其中國內為149個。從適應癥來看,2型糖尿病治療仍然是GLP-1類藥物的主要研究方向,布局了減肥適應癥的藥物多達93個,其中也包括多家中國藥企。
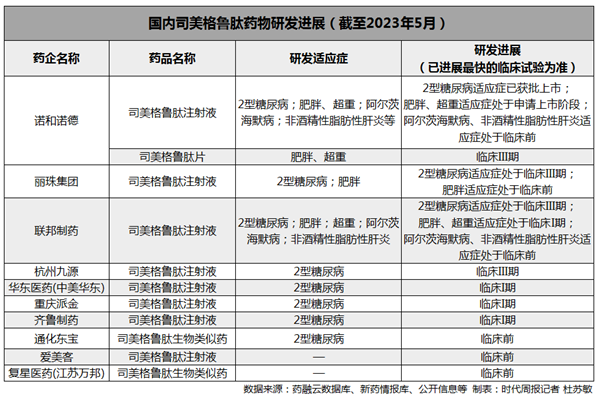
創新藥企業眾生睿創高管劉文(化名)在接受時代周報記者采訪時表示,目前國內有上百家企業在針對GLP-1靶點進行開發,“我們不是做單靶點的,而是雙靶點,對標的也并非司美格魯肽,而是禮來的替爾泊肽(Tirzepatide)。目前GLP-1賽道的方向是長效化、多靶點。”據劉文透露,目前公司的GLP-1藥物已進入臨床階段,投入的研發經費“已經有幾千萬元了”。
據摩根士丹利估算,到2030年,肥胖藥物的市場規模預計超過540億美元(合約人民幣3848億元),有望超過PD-1/PD-L1成為全球市場規模最大的品類。同樣正在開發GLP-1靶點的口服減肥藥的輝瑞制藥(PFE.NYSE)則預測,在不到十年的時間內,GLP-1藥物總市場規模可能接近1000億美元,成為新一代“藥王”。
而在GLP-1藥物的賽道上,則呈現出“雙雄爭霸,巨頭環伺”的局面。諾和諾德和禮來兩大國際藥企處于無可爭議的第一梯隊。
據藥智全球暢銷藥品銷售數據庫,諾和諾德研發的司美格魯肽系列藥物在2022年實現銷售額109億美元,與2021年的61億美元相比,增幅高達78%,成為了首個年銷售額破百億美元的GLP-1類藥物,在全球暢銷藥品中排名第七。另一家藥企巨頭禮來(LLY.NYSE)的GLP-1R藥品度拉糖肽則在2022年斬獲74億美元(約合人民幣527.34億元)。
5月4日,諾和諾德發布的2023年一季度財報顯示,報告期內,司美格魯肽三個劑型合計貢獻了42.4億美元。其中,降糖藥司美格魯肽注射液Ozempic銷售額為29.1億美元;口服降糖藥司美格魯肽片Rybelsus銷售額為6.5億美元;減肥藥司美格魯肽注射液Wegovy銷售額為6.7億美元。
而諾和諾德的口服版減肥藥司美格魯肽片更是備受市場關注,近期其臨床試驗也迎來了新進展。5月22日,諾和諾德公布了司美格魯肽50mg片劑的OASIS1三期臨床研究數據。數據顯示,患者的平均基線體重為105.4kg,50mg組患者的體重減輕17.4%。
“我們對GLP-1類藥物充滿信心。我們是GLP-1領域的先行者和領導者,將繼續引領創新突破,造福糖尿病、乃至更多疾病領域的患者。”諾和諾德相關負責人告訴時代周報記者。
諾和諾德的“老對手”禮來也于2022年9月在國內申報旗下產品替爾泊肽上市,用于在飲食控制和運動基礎上改善成人2型糖尿病患者的血糖控制。
三
“新貴”挑戰“舊王”
在國內藥企中,華東醫藥可謂是對GLP-1賽道進攻態勢最猛的一個。
2023年3月,華東醫藥曾發布公告稱,由子公司中美華東申報的利拉魯肽注射液“適用于成人2型糖尿病患者控制血糖”的上市許可申請獲得批準,商品名為利魯平,成為國內首個率先搶灘利拉魯肽市場的藥企。據時代周報記者梳理,復星醫藥(600196.SH)旗下江蘇萬邦、愛美客(300896.SZ)等在研的利拉魯肽生物類似藥已處于臨床階段。
據華東醫藥官方公眾號,2023年5月,華東醫藥舉辦了“利魯平”利拉魯肽注射液上市發布會,并邀請多家連鎖藥店負責人參會。中美華東院外事業部總監代陽在會上表示,目前公司院外團隊近800人,院外銷售規模、核心產品的終端覆蓋率正穩步提升,將一以貫之加大院外市場布局力度。據媒體報道,中美華東的利拉魯肽注射液還在阿里健康和京東健康線上首發。時代周報記者檢索發現,3ml/支的利魯平最低價為199元/盒,同劑量由諾和諾德出品的諾和力最低價約為260元/盒。
從上述舉動可以看出,華東醫藥正在發力利魯平的線上線下全渠道鋪設。
而華東醫藥的野心也遠不止降糖市場。在上述會議上,浙江省中醫院內分泌科主任、主任醫師倪海祥在《因勢利導 不止于平糖》的演講中表示,利魯平生產過程符合cGMP要求,海外授權,國際品質,是國內第一個利拉魯肽生物類似藥,與原研等效,有望成為第一個具有減肥適應癥的降糖藥。據其PPT顯示,利魯平的減肥適應癥預計將于2023年底獲批。
 △ 圖片來源:華東醫藥官方公眾號
△ 圖片來源:華東醫藥官方公眾號
除了利拉魯肽外,華東醫藥還是首個挑戰諾和諾德司美格魯肽中國專利的國內藥企。
華東醫藥于2021年6月10日向國家知識產權局遞交司美格魯肽專利無效申請。2022年9月5日,國家知識產權局判定司美格魯肽核心專利(CN200680006674.6)全部無效。對此,諾和諾德在2022年財報中表示,已上訴至北京知識產權法院,后續將進入知識產權訴訟階段。
李鳴向時代周報記者分析時表示,挑戰成功的原因可能是諾和諾德關于司美格魯肽的專利覆蓋面太廣,關鍵結構未進行充分的數據論證,被華東醫藥抓住了機會。此外,也有業內分析人士在接受媒體采訪時指出,諾和諾德因為出于保密等考慮并未在實施例中給出具體化合物的實驗結果數據,因此成為了華東醫藥挑戰其專利的突破口。
這是否意味著諾和諾德失去了司美格魯肽在中國的專利保護?一位從事知識產權業務的律師告訴時代周報記者,在訴訟期間專利仍處于有效狀態,如果訴訟雙方對判決結果不滿,還可以進一步上訴至最高人民法院。諾和諾德在2022年財報中表示,其司美格魯肽注射液在中國的專利正常于2026年到期。
目前,華東醫藥的司美格魯肽注射液仿制藥已進入臨床I期,用于2型糖尿病患者的血糖控制。
6月1日,時代周報就利魯平銷售渠道、司美格魯肽專利訴訟相關事宜致電華東醫藥董秘辦并發去采訪郵件,截至發稿前未收到回復。就目前雙方的訴訟進展問題,諾和諾德相關負責人回復時代周報記者稱“具體細節不方便評論”。
對于國內藥企而言,加速搶仿司美格魯肽是當前重點,因為彎道超車的時間窗口僅剩兩年多。“我估計諾和諾德會一直糾纏下去,直到過期,畢竟還可以起訴專利局,拖一拖也就耗到過期了。此外,司美格魯肽的減肥適應癥如果批了,仿制藥若走適應癥拓展的方式,也就是直接證明自己與前者質量一致,不用做臨床就能上市也是有可能的。”李鳴分析道。
編者按:本文轉載自微信公眾號:時代周報(ID:timeweekly),作者:杜蘇敏 、鄧宇晨

前瞻經濟學人
專注于中國各行業市場分析、未來發展趨勢等。掃一掃立即關注。




























