1個(gè)回答
-
邀請(qǐng)演講a)產(chǎn)業(yè)政策
單抗行業(yè)為生物產(chǎn)業(yè)的重要組成部分,近年政府出臺(tái)了系列政策鼓勵(lì)和支持本行業(yè)的發(fā)展。
圖表1:生物單抗藥相關(guān)政策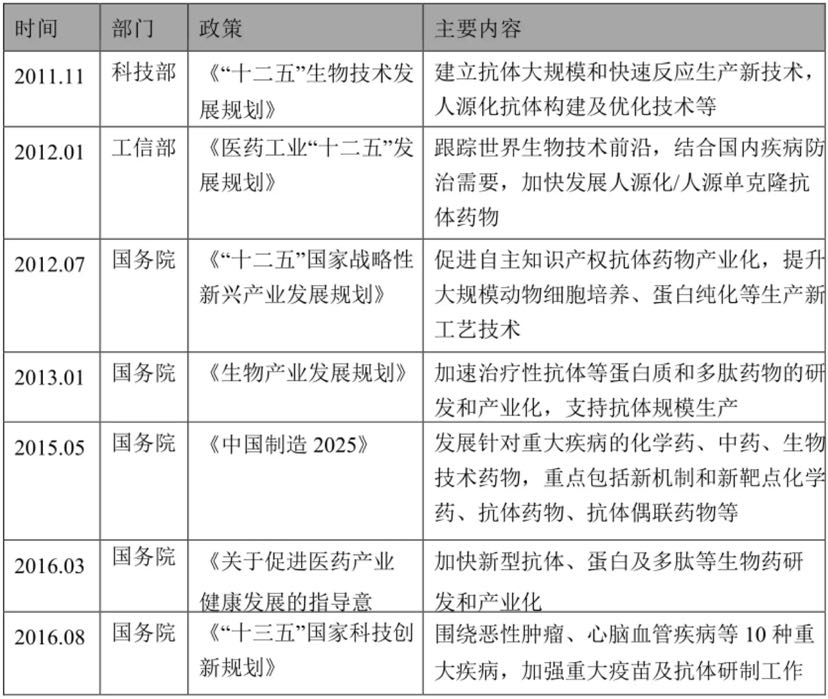
資料來源:前瞻產(chǎn)業(yè)研究院整理
b)醫(yī)保政策
中國人力資源和社會(huì)保障部7月19日宣布,新增36種藥品經(jīng)談判成功正式納入國家基本醫(yī)療保險(xiǎn)、工傷保險(xiǎn)和生育保險(xiǎn)藥品目錄乙類范圍。其中包含了5個(gè)單抗品種和1個(gè)融合蛋白,被納入醫(yī)保乙類范圍之后,藥品價(jià)格大幅下降。此前這些藥品臨床價(jià)值高但價(jià)格較貴,患者負(fù)擔(dān)重。如乳腺癌靶向藥曲妥珠單抗,2016年國內(nèi)市場價(jià)格約為每單位24500元。此次談判后,曲妥珠單抗進(jìn)入醫(yī)保藥品目錄后的支付標(biāo)準(zhǔn)降至每單位7600元,降幅約為69%。考慮到進(jìn)入乙類目錄后,醫(yī)保基金將支付70%多的費(fèi)用,患者個(gè)人負(fù)擔(dān)的費(fèi)用進(jìn)一步減輕。這次醫(yī)保目錄的調(diào)整對(duì)國產(chǎn)單抗是一大利好。
c)藥品審評(píng)審批政策
長期以來,我國新藥審評(píng)耗時(shí)冗長,嚴(yán)重制約了創(chuàng)新藥的發(fā)展,國家局現(xiàn)已意識(shí)到問題的嚴(yán)峻并著力解決。2015年8月,國務(wù)院發(fā)布《改革藥品醫(yī)療器械審評(píng)審批制度的意見》,明確將加快創(chuàng)新藥的審評(píng)審批,對(duì)創(chuàng)新藥實(shí)行特殊審評(píng)審批制度。2017年10月,中共中央辦公廳、國務(wù)院辦公廳印發(fā)《關(guān)于深化審評(píng)審批制度改革鼓勵(lì)藥品醫(yī)療器械創(chuàng)新的意見》,單抗藥物作為創(chuàng)新藥的重要組成部分,也將受益于此次藥審改革。
G 評(píng)論掃一掃
打開app查看精彩評(píng)論 收藏
收藏掃一掃
打開app查看精彩評(píng)論

掃一掃
下載《前瞻經(jīng)濟(jì)學(xué)人APP》進(jìn)行提問
與資深行業(yè)研究員/經(jīng)濟(jì)學(xué)家互動(dòng)交流讓您成為更懂行業(yè)的人






























